INFECCIÓN DE HERIDA QUIRÚRGICA Y PROFILAXIS ANTIBIÓTICA
INTRODUCCIÓN
La infección posoperatoria de la herida quirúrgica es la mayor causa de morbilidad infecciosa en el paciente quirúrgico. Ocasiona prolongadas estadías hospitalarias, incremento de los costos de la atención médica y serios inconvenientes a los pacientes y sus familiares.
En la década del 70 se establecieron con claridad las indicaciones de profilaxis y sus ventajas. Su objetivo es la disminución de la morbimortalidad por infecciones posquirúrgicas y/o de heridas. La administración de antibióticos, sin embargo, es un complemento de las medidas de prevención en infecciones quirúrgicas.
Definición de infección de herida quirúrgica
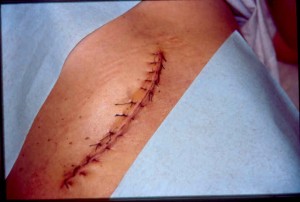 Aquella que ocurre a partir de la contaminación bacteriana causada por un procedimiento quirúrgico. Aunque la definición se circunscribe solamente a la “herida” quirúrgica, se extiende también a la afectación de tejidos más profundos involucrados en el procedimiento operatorio, y que suelen estar libres de gérmenes en condiciones normales.
Aquella que ocurre a partir de la contaminación bacteriana causada por un procedimiento quirúrgico. Aunque la definición se circunscribe solamente a la “herida” quirúrgica, se extiende también a la afectación de tejidos más profundos involucrados en el procedimiento operatorio, y que suelen estar libres de gérmenes en condiciones normales.
Para definir el tipo de infección postquirúrgica debe tomarse en cuenta el tipo de herida con la clasificación de los siguientes criterios de acuerdo a la Norma Oficial Mexicana (NOM-EM-002-SSA2-2003):
Limpia.
- Cirugía electiva con cierre primario y sin drenaje.
- No traumática y no infectada.
- Sin “ruptura” de la técnica aséptica.
- No se invade el tracto respiratorio, digestivo ni genito-urinario.
Limpia-contaminada.
- La cirugía se efectúa en el tracto respiratorio, digestivo o genito-urinario bajo condiciones controladas y sin una contaminación inusual.
- Apendicectomía no perforada.
- Cirugía del tracto genito-urinario con urocultivo negativo.
- Cirugía de la vía biliar con bilis estéril.
- Rupturas en la técnica aséptica sólo en las cirugías contaminadas.
- Drenajes (cualquier tipo).
Contaminada.
- Herida abierta o traumática.
- Salida de contenido gastrointestinal.
- Ruptura de la técnica aséptica sólo en las cirugías contaminadas.
- Incisiones en tejido inflamado sin secreción purulenta.
- Cuando se entra al tracto urinario o biliar y cuando la orina o la bilis están infectados.
Sucia o infectada.
- Herida traumática con tejido desvitalizado, cuerpos extraños, contaminación fecal, con inicio de tratamiento tardío o de un origen sucio.
- Perforación de víscera hueca.
- Inflamación e infección aguda (con pus), detectadas durante la intervención.
Infección de herida quirúrgica incisional superficial.
Ocurre en el sitio de la incisión dentro de los 30 días posteriores a la cirugía y que solamente involucra piel y tejido celular subcutáneo del sitio de la incisión.
Con uno o más de los siguientes criterios:
- Drenaje purulento de la incisión superficial.
- Cultivo positivo de la secreción o del tejido obtenido en forma aséptica de la incisión.
- Presencia de por lo menos un signo o síntoma de infección con cultivo positivo.
- Herida que el cirujano deliberadamente abre (con cultivo positivo) o juzga clínicamente infectada y se administran antibióticos.
Infección de herida quirúrgica incisional profunda.
Es aquella que ocurre en el sitio de la incisión quirúrgica y que abarca la fascia y el músculo y que ocurre en los primeros 30 días después de la cirugía si no se colocó implante, o dentro del primer año si se colocó implante.
Con uno o más de los siguientes criterios:
- Secreción purulenta del drenaje colocado por debajo de la aponeurosis.
- Una incisión profunda con dehiscencia, o que deliberadamente es abierta por el cirujano, acompañada de fiebre o dolor local.
- Presencia de absceso o cualquier evidencia de infección observada durante los procedimientos diagnósticos o quirúrgicos.
- Diagnóstico de infección por el cirujano o administración de antibióticos.
Infección de órganos y espacios.
Involucra cualquier región (a excepción de la incisión), que se haya manipulado durante el procedimiento quirúrgico. Ocurre en los primeros 30 días después de la cirugía si no se colocó implante, o dentro del primer año si se colocó implante. Para la localización de la infección se asignan sitios específicos (hígado, páncreas, conductos biliares, espacio subfrénico o subdiafragmático, o tejido intraabdominal).
Con uno o más de los siguientes criterios:
- Secreción purulenta del drenaje colocado por el contra-abertura en el órgano o espacio.
- Presencia de absceso o cualquier evidencia de infección observada durante los procedimientos diagnósticos o quirúrgicos.
- Cultivo positivo de la secreción o del tejido involucrado.
- Diagnóstico de infección por el cirujano o administración de antibióticos.
PATOGENIA
Las infecciones de las heridas quirúrgicas dependen de varios factores: relacionados al paciente y sus enfermedades subyacentes; al tipo de procedimiento y si hay implantación de material extraño al hospedero; de la magnitud del trauma quirúrgico; del tipo de microorganismo y su capacidad de adherencia y de la profilaxis antimicrobiana peri operatoria.
Casi todas las infecciones de heridas quirúrgicas se adquieren en el momento de la intervención mediante la implantación de los microorganismos provenientes de un reservorio o fuente, en el campo operatorio, al momento de la cirugía.
La mayoría de los microorganismos infectantes a las heridas quirúrgicas son transmitidos desde algún área de la superficie corporal del paciente, adyacente a la herida, o de lugares distantes al quirófano. Los reservorios o fuentes más importantes de contaminación lo constituyen el personal, los pacientes y el ambiente hospitalario. Un reservorio potencial de microorganismos lo constituyen las manos del trabajador de la salud involucrado en el cuidado del paciente, así como el cabello y cuero cabelludo del personal de salud.
El tracto respiratorio no representa una fuente importante y común de microorganismos responsables de infecciones de heridas quirúrgicas, la mayoría de las infecciones son causadas por microorganismos de la flora normal de la piel, vísceras huecas y de las mucosas del mismo paciente. El ambiente operatorio es causa muy rara de infección postoperatoria cuando se cumplen con todas las condiciones adecuadas de mantenimiento y limpieza. Los reservorios inanimados responsables de infecciones de heridas operatorias son los antisépticos contaminados, los apósitos o material contaminado. La forma de transmisión de los gérmenes puede ser por contacto directo a través de las manos contaminadas, o indirecto a través de gotas o partículas que pueden tener bacterias.
ETIOLOGÍA
La mayoría de las infecciones de las heridas quirúrgicas son causadas por bacterias y las más comúnmente aisladas son los Gram positivos (S. aureus, Enterococcus spp, S. coagulasa negativa) y algunos gérmenes Gram negativos principalmente E. coli. También pueden encontrarse otros Gram negativos con menor frecuencia como Enterobacter spp, P. mirabilis, K. pneumoniae, P. aeruginosa.
La etiología de las infecciones de herida quirúrgica también está en relación al tipo de cirugía y órgano intervenido, así en cirugías de colon puede predominar E. coli y Bacteroides fragilis.
PROFILAXIS ANTIBIÓTICA
La profilaxis se define como la administración de antibióticos en ausencia de infecciones sospechadas o corroboradas con la finalidad de disminuir las complicaciones infecciosas asociadas a una determinada situación, en este caso un procedimiento quirúrgico.
En cualquier situación donde se administre profilaxis antibiótica los beneficios deben superar al perjuicio (efectos adversos, resistencias, costos)
La profilaxis antibiótica quirúrgica supone un aproximado del 30% de todos los antibióticos administrados en un hospital general, y hasta un 80% en las salas de hospitalización quirúrgicas. Se estima que hasta un 70% de la profilaxis quirúrgica es mal utilizada, bien sea por su Indicación para profilaxis, antibiótico seleccionado, tiempo de inicio o duración de la misma.
En 1961 Burke demuestra la relación que hay entre el tiempo de administración del antibiótico y su eficacia profiláctica. Se determina que para prevenir las posteriores infecciones el antibiótico debe estar presente en los tejidos antes o en el momento de la contaminación bacteriana.
Indicaciones para profilaxis
Tiene que haber una indicación adecuada, donde se haya comprobado su efectividad en disminuir la incidencia de infecciones. La profilaxis con antibióticos está justificada en las cirugías que tienen un alto índice de infección (mayor al 5 al 10%) o donde la infección como complicación podría producir consecuencias catastróficas (cardiovascular, neurocirugía, prótesis ortopédicas).
Las consecuencias de la profilaxis antibiótica inadecuada incluyen mayores costos económicos por los antibióticos utilizados innecesariamente, la aparición de bacterias resistentes, o selección de ellas y efectos adversos de los antibióticos (reacciones alérgicas, toxicidad).
Clasificación de las heridas quirúrgicas y el riesgo de infección.
Cirugía limpia: riesgo de infección 1 a 5%, no está indicada la profilaxis antibiótica con excepción de cirugías cardiovasculares, ortopédicas con implantación de prótesis o material de fijación y neurocirugías.
Limpia contaminada: riesgo de infección del 5 al 15%. Indicación de profilaxis antibiótica
Contaminada: riesgo de infección del 15 al 40%. Indicación de profilaxis antibiótica
Cirugía Sucia o infectada: Riesgo de infección mayor al 40% (si no está infectada). Administración de antibióticos con fin terapéutico y no profiláctico
Antibiótico
La selección del antibiótico debe estar basada en los patógenos bacterianos que mas probablemente originarán complicaciones infecciosas del método quirúrgico especifico, el perfil de sensibilidad de tales patógenos, la inocuidad, eficacia y costos económicos de cada medicamento. Por lo común no se recomienda administrar los antibióticos nuevos, más caros y de mayor espectro, salvo que hayan demostrado que su eficacia profiláctica es mejor que la de los medicamentos cuyo beneficio está bien definido.
Los antibióticos no tienen que ser activos contra todos los posibles microorganismos. No se recomienda el uso rutinario de vancomicina ni de cefalosporinas de amplio espectro
Por lo general, los antibióticos profilácticos se proponen como monoterapia, salvo en situaciones donde la sospecha de infecciones sea por múltiples gérmenes, como en el caso de traumatismo penetrante abdominal, cirugía de colon o abdominal de emergencia donde se espera encontrar flora mixta.
Momento de administración
La profilaxis se administra antes del procedimiento quirúrgico, y no posterior a este. La profilaxis se logra cuando existen adecuadas concentraciones de antibiótico en tejidos al momento de la contaminación bacteriana (incisión quirúrgica) con administración no mayor de 2 hrs antes del procedimiento quirúrgico y no menor de 30 minutos, por lo que la administración de la profilaxis antibiótica 1 hora antes de la incisión quirúrgica resulta adecuada
Duración de la profilaxis
Para la mayoría de las cirugías basta una sola dosis de antibiótico profiláctico que logre concentraciones tisulares adecuadas durante el procedimiento quirúrgico.
Es recomendable administrar una segunda dosis durante el transoperatorio cuando se utilizan antibióticos de vida media breve, cuando el procedimiento quirúrgico se prolonga más 4 horas o cuando exista sangrado masivo durante el procedimiento.
En la realización de cirugías contaminadas que involucre vísceras con elevada carga bacteriana como es el caso de cirugías colo-rectales la profilaxis se podrá extender por 3 dosis o 24 horas en el postoperatorio pero nunca más de este periodo de tiempo.
En el caso de las cirugías cardiovasculares se recomienda extender la profilaxis antibiótica por 48 horas (algunos expertos recomiendan prolongar la profilaxis hasta retirar todos los drenajes torácicos).
Vía de administración
La vía de administración intravenosa es la única que logra niveles sanguíneos fiables durante la cirugía para la realización de profilaxis de infección de herida quirúrgica. Los niveles que se consiguen mediante las vías oral o intramuscular dependen de factores que varían entre individuos por lo que las hacen unas vías inseguras.
Esquemas antibióticos profilácticos recomendados
La cefalotina es una cefalosporina de primera generación adecuada para la mayoría de las profilaxis quirúrgicas, tiene excelente cobertura contra S. aureus, y aceptable cobertura contra Enterobacterias (E. coli, Klebsiella sp.). No se justifica el uso profiláctico de vancomicina ya que en nuestra institución (HIT) el porcentaje de SAMR (Staphylococcus aureus meticilino resistente) es menor al 15% (febrero 2011)
Antes de administrar la profilaxis antibiótica realizar una correcta clasificación del procedimiento quirúrgico que se va a realizar ya que para la mayoría de las cirugías limpias no se requiere profilaxis, con excepciones en cirugías ortopédicas, cardiovasculares y neurocirugía. En cirugías sucias o infectadas no se realiza profilaxis sino tratamiento antibiótico, pero de igual manera el antibiótico se administra previo al procedimiento quirúrgico.
Cirugía cardiovascular
Cefalotina 50 mg/kg/dosis en el preoperatorio y luego 100 mg/kg/día IV cada 6 horas por 48 horas (algunos expertos recomiendan hasta retirar tubos de drenaje)
Cirugía ortopédica
En las cirugías de colocación de prótesis o material de fijación de fracturas Cefalotina 50 mg/kg/dosis en el preoperatorio.
En el caso de amputación de miembros inferiores se recomienda el uso de Clindamicina 15 mg/kg/dosis
En el caso de fracturas expuestas no está indicada la profilaxis sino el tratamiento antibiótico.
Neurocirugía
Craneotomía, cirugías con colocación de sistema de derivación de LCR y otras cirugías limpias Cefalotina 50 mg/kg/dosis en el preoperatorio.
Cirugías a través de senos paranasales o mucosa orofraingea clindamicina 10 mg/kg/dosis + gentamicina 2.5 mg/kg/dosis
Cirugía de cabeza y cuello
Las cirugías limpias no necesitan profilaxis antibiótica
Si se realiza incisión a través de la mucosa oral, o mucosa ótica utilizar Clindamicina 10 mg/kg/dosis asociada a aminoglucósido (Gentamicina 2.5 mg/kg/dosis o Amikacina a 7.5 mg/kg/dosis)
Cirugía esofágica y gastroduodenal
Cefalotina 50 mg/kg/dosis en el preoperatorio.
En el caso de atresia esofágica Clindamicina 10 mg/kg/dosis asociada a Gentamicina 2.5 mg/kg/dosis
Cirugía de vías biliares
En situaciones donde exista obstrucción de la vía biliar (quiste de colédoco, atresia de vías biliares o cálculos, etc.) Cefalotina 50 mg/kg/dosis en el preoperatorio o Clindamicina 10 mg/kg/dosis asociada a Gentamicina 2.5 mg/kg/dosis
Cirugía urológica
Es importante realizar un urocultivo previo al acto quirúrgico. En caso de ser positivo, el paciente deberá recibir tratamiento con el antibiótico adecuado previo a la cirugía.
Se recomienda la profilaxis en el caso de obstrucción o instrumentación urológica (litiasis, plastía ureteral, implantación ureteral) cefalotina 50 mg/kg/dosis en el preoperatorio.
En pacientes que vienen recibiendo profilaxis con antibióticos orales, utilizar cefalosporinas de 3era generación (Ceftriaxona o Cefotaxima 50 mg/kg/dosis).
Patología apendicular
Todo paciente con apendicitis que va a ser sometido a cirugía debe recibir profilaxis quirúrgica.
1.- Clindamicina 10 mg/kg/dosis asociado a aminoglucósido (Gentamicina 2.5 mg/kg/dosis o Amikacina 7.5 mg/kg/dosis) durante 24 horas
2.- Metronidazol 10 mg/kg/dosis asociado a aminoglucósido (Gentamicina 2.5 mg/kg/dosis o Amikacina 7.5 mg/kg/dosis) durante 24 horas
No se requiere cobertura inicial contra enterococo excepto en inmunocomprometidos o pacientes con tratamiento antibiótico de amplio espectro previo, en este caso se agregara Ampicilina 50 mg/kg/dosis.
De acuerdo al informe del cirujano, se determinará si se suspenden los antibióticos a las 24 hs (Apéndice No perforada) o si se completará un tratamiento de 5 a 7 días (Apéndice perforada)
Cirugía colorrectal
1.- Clindamicina 10 mg/kg/dosis asociado a aminoglucósido (Gentamicina 2.5 mg/kg/dosis o Amikacina 7.5 mg/kg/dosis) durante 24 horas
2.- Metronidazol 10 mg/kg/dosis asociado a aminoglucósido (Gentamicina 2.5 mg/kg/dosis o Amikacina 7.5 mg/kg/dosis) durante 24 horas
Opcionalmente lavados intestinales a criterio del cirujano y administración de neomicina 25 mg/kg/dosis mas eritromicina 10 mg/kg/dosis administrados 19 hs, 18 hs y 11 hs antes de la cirugía
No se requiere cobertura inicial contra enterococo, excepto en inmuno comprometidos o pacientes con tratamiento antibiótico previo de amplio espectro, en este caso se agregara Ampicilina 50 mg/kg/dosis
Cirugía neonatal (Neonatos de <72 horas de vida)
Ampicilina 50 mg/kg/dosis asociado a Gentamicina 2.5 mg/kg/dosis
En general la Gentamicina puede ser sustituida por la Amikacina y viceversa. Considerar la sustitución del aminoglucósido por una Cefalosporina de 3era generación (Ceftriaxona) en pacientes con alteración en la función renal y en pacientes con estancia hospitalaria prolongada. No se recomienda el uso de un betalactámico (Cefalosporina) asociado a un aminoglucósido (Amikacina, Gentamicina) ya que lejos de traer un beneficio terapéutico solo se aumentan los efectos adversos (ototoxicidad, nefrotoxicidad), de continuar un tratamiento con aminoglucósido se deberá administrar como monodosis cada 24 hrs.
En caso de alergia a penicilinas, tomando en consideración que el 90% de las personas que se dicen alérgicas a la penicilina realmente no lo son, solo se recomienda utilizar un fármaco diferente a los betalactamicos en pacientes con historia de reacción alérgica tipo I (anafiláctica) en cuyo caso está justificado el uso de vancomicina para cobertura de S. aureus, otra alternativa es la Clindamicina, recordando que ninguno de los 2 antibióticos anteriores cubre bacilos Gram negativos a diferencia de la cefalotina.
Si se presenta una infección de herida quirúrgica en un paciente en el que se utilizó profilaxis antibiótica, por lo general los microorganismos involucrados son susceptibles a los mismos antibióticos utilizados durante la profilaxis.
La profilaxis antibiótica no sustituye ninguna de las medidas de asepsia ni una adecuada técnica quirúrgica